文|氨基觀察 黃愷
雖然在全球創新藥領域,國內藥企起步并不早,目前尚處于追趕階段,但一個不可否認的事實是,它們的站位正越來越居前。
這一點,在諸多療法領域已經得到了充分的證明。典型如ADC浪潮下,國內藥企依靠工程師等綜合優勢,占據上風。
不僅是ADC,在細胞療法領域,國內藥企也處于領先身位。例如,在CAR-T療法的紅斑狼瘡適應癥的探索中,許多國內選手的研發進度跑到了海外大藥企的前面。
那么,在這場遲遲未能被攻克的疾病領域,率先突圍的會是中國藥企嗎?
01 尚無根治療法的窘境

作為一種自身免疫系統帶來的疾病,紅斑狼瘡是實實在在的“存在巨大未滿足臨床需求”領域。
從發病機制來看,其誘因是患者的血清中存在多種自身抗體,并結合自身抗原形成抗原抗體免疫復合物,沉積在不同組織并引起相應的免疫反應,造成多系統損傷。
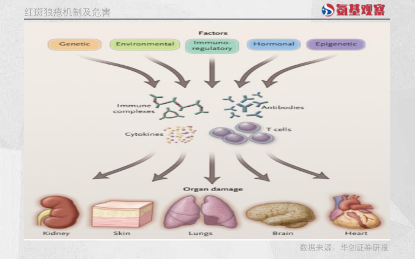
紅斑狼瘡最具特征的癥狀是面頰部出現蝶形紅斑,而“狼瘡”的名字正是因為過去人們認為該病的面部紅斑表現,像是被狼咬傷所致。而除了皮膚損害,紅斑狼瘡的病變還可累及多臟器和系統。
這也導致,患者會隨著患病周期加長而處于病情加速惡化的處境。目前,患者的10年生存率雖已升至目前的97%,但25-30年后的存活率呈斷崖式下降,僅為30%。因此,紅斑狼瘡患者存在著極強的治療需求和迫切的治愈意愿。
但遺憾的是,現有治療藥物,均無法起到根治的效果,只能是起到短期控制疾病活動的作用。
在無治愈療法的情況下,當前常用糖皮質激素、抗瘧藥、免疫抑制劑和生物制劑等進行紅斑狼瘡的治療。而這些療法無一例外,效果欠佳且存在副作用較高的bug。
如下圖所示,糖皮質激素是治療紅斑狼瘡的基礎用藥,以激素為基礎的傳統療法仍存在反應率不足、復發風險高、副作用明顯等問題。

總的來說,紅斑狼瘡藥物的研發方向極為確定。
其中,治療的短期目標是控制疾病活動、改善臨床癥狀、達到臨床緩解或可能達到的最低疾病活動度;
長期目標,則主要為預防和減少復發,減少藥物不良反應,預防和控制疾病所致的器官損害,實現病情長期持續緩解,降低患者病死率,提高患者的生活質量。
盡管方向明確,但紅斑狼瘡藥物的研發并不容易。
02 需要翻越的兩座大山
對于紅斑狼瘡藥物的研發來說,核心困境是兩座大山難以翻越:發病機制和臨床設計。
發病機制方面,該病的病因至今尚未確定。
雖然我們能夠發現,自身免疫系統的過度激活,導致了紅斑狼瘡的存在。但,又是什么因素導致自身免疫系統的過度激活,尚無定論。
當前,學術界普遍認為遺傳、內分泌、感染和環境等因素均與發病有關。研究仍在繼續,目前甚至有人正在研究齲齒與紅斑狼瘡之間的關系。
因此,我們要想明確免疫系統激活驅動因素,進而達到對癥治療,預防臨床疾病的發生仍不現實。
除了機制不明這一因素,“煉獄”級別的臨床難度,也是阻礙新療法面世的因素之一。
因為疾病的特殊性,不同的人群、適應癥以及藥物給藥劑量的設定,都會直接影響臨床的成敗。
由于紅斑狼瘡具有高度“變異性”,不同的患者會有各自不同的癥狀。在此前紅斑狼瘡新藥研發的過程中,臨床評價環節成了眾多候選藥物難以翻越的一座大山。
另外,因為紅斑狼瘡病情多不穩定、變化快,醫生在治療時尤為謹慎。出于安全性考慮,采用什么劑量、多久給一次藥,都是有待解決的難題。
諸多因素導致,紅斑狼瘡堪稱創新藥研發黑洞。截至目前,上市的有效藥物寥寥無幾。
03 加速向前的攻堅戰
當然,我們對于紅斑狼瘡的攻堅戰,并非一無所獲。
即便對于最終驅動免疫系統過度激活的因素尚不得知,但基于對免疫系統細胞、介質和途徑對狼瘡發病機制的了解,具有靶向性的生物藥開始走向臺前。
截至目前,全球有多款大分子藥物上市,包括葛蘭素史克的貝利尤單抗、榮昌生物的泰它西普、阿斯利康的阿伏利尤單抗等。
相比于傳統藥物,靶向性藥物由于能夠高特異性結合靶點,減少全身性副作用發生,提
高治療窗口從而提升療效和安全性。因此,上市已久的貝利尤單抗早就邁入重磅炸彈行列,2021年上市的伏利尤單抗也同樣快速放量,今年前三季度銷售額接近2億美金。
與此同時,包括JAK抑制劑、CD20單抗等諸多創新療法,均已進入注冊臨床階段。不遠的將來,我們將會迎來更多紅斑狼瘡的新療法。
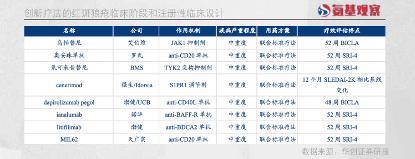
當然,這些藥物都還不是勝利的終點。
當前已經上市的靶向藥物,臨床定位主要是此前療法的補充,主要應用場景,是對難治性(經常規治療效果不佳)或復發性紅斑狼瘡患者在標準療法的基礎上起到改善作用。
從臨床設計來看也是如此。根據現有上市的大分子藥物,臨床主要納入的患者群體為中重度SLE患者,治療時需聯合標準療法。

并且,療效評估指標多為SRI-4或BICLA,僅反映了用藥后相比基線患者疾病活動的改善,而未衡量“治愈或接近治愈”的指標,例如達到DORIS(系統性紅斑狼瘡緩解定義工作組)緩解或LLDAS(低疾病活動度)的患者比例。

這是因為,相比DORIS緩解或者LLDAS,當前臨床設置的主要終點都更容易達到。以貝利尤單抗為例,回顧性分析結果顯示,BLISS-52和BLISS-76兩項臨床中,DORIS緩解的比例僅為5-6%,LLDAS達標率也僅為12-15%。
實際上,上述提到的多款處于研發后期階段的生物制劑或靶向小分子藥物,定位也是緩解疾病活動,而并非“無藥物完全緩解”的狀態。
很顯然,這場攻堅戰能要繼續向前。
04 CAR-T療法會是最終答案嗎?
或許,CAR-T療法能給我們帶來更大驚喜。
從機制來看,系統性紅斑狼瘡的發病和進展和B細胞密切相關,因此靶向B細胞的療法一直是研發的重要方向。
此前靶向B細胞的療法,由于無法徹底清除B細胞或無法完全抑制B細胞活性等因素導致,難以達到治愈的結果,而CAR-T療法則具有這一可能。
CAR-T療法能夠通過表達CD19 CAR特異性殺傷B細胞,或通過表達BCMA CAR特異性殺傷B細胞分化而來的漿細胞,從而有望達到深度清除紅斑狼瘡致病性B細胞的效果,觸發免疫“重置(reset)”,完全緩解紅斑狼瘡疾病。
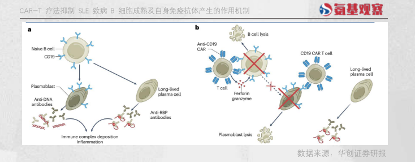
隨著美國田納西州大學健康科學中心的科學家,于2019 年在小鼠模型中驗證了這一可能之后,CAR-T療法應用于紅斑狼瘡治療的研究邁入快車道。
ASH 2023年會上,Georg Schett 團隊更新的研究數據顯示出良好的效果。8例紅斑狼瘡患者在接受治療3個月后達到完全緩解,此后SLEDAI維持0分。5例隨訪14-24個月的紅斑狼瘡患者B細胞已經重建,病情仍維持緩解。
不僅是海外研究,中山市人民醫院研究團隊也展開了類似的研究,得出的結論也是一致:CAR-T療法治療紅斑狼瘡有望安全高效達到一次性治愈。
這無疑是紅斑狼瘡患者新的希望。當然,結論是否正確還有待藥企們繼續攻堅。截至目前,包括諾華等全球多家企業均入局了CAR-T療法在紅斑狼瘡領域的探索。
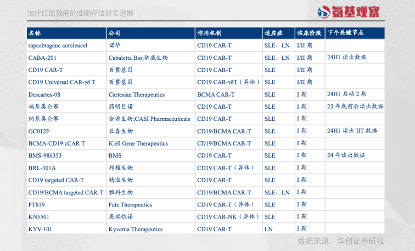
其中,國內藥企為中堅力量。如上圖所示,包括馴鹿生物、百暨基因、藥明巨諾、合源生物等均有所布局,不管是布局數量還是進度層面,國內藥企都處于領先身位。
那么,國內藥企會率先脫穎而出嗎?讓我們拭目以待。



