文|MedTrend醫(yī)趨勢
墻內(nèi)開花墻外香。
嵌合抗原受體T細胞(CAR-T)療法是近年來癌癥治療領(lǐng)域一顆耀眼的明星。不僅在血液腫瘤中建樹頗豐,在攻克實體瘤的方向上也邁出了重要一步。過去十年間,CAR-T療法在中國快速發(fā)展,臨床試驗注冊數(shù)量及發(fā)表文獻量持續(xù)攀升。
截至2024年12月31日,中國已有6款商業(yè)化CAR-T細胞產(chǎn)品獲批,其中3款靶向CD19、3款靶向BCMA。其中2024年,傳奇生物的核心產(chǎn)品CAR-T細胞療法西達基奧侖賽注射液在全球市場大放異彩,銷售額高達9.63億美元,距離“重磅炸彈”藥物10億美元標準僅一步之遙。
但是國產(chǎn)CAR-T療法的日子,并不好過。這種艱難在近期“傳奇生物裁撤中國商業(yè)化、GMP團隊”(傳奇生物裁撤中國商業(yè)化、GMP團隊?)的消息中,被聚焦放大。
不獨傳奇生物,另一家明星公司藥明巨諾也發(fā)布2024年財報:全年營收1.58億元,同比下滑9%,虧損額為5.9億元。據(jù)悉目前賬上現(xiàn)金撐不過兩年。
為什么會出現(xiàn)這樣的反差?
一方面,CAR-T細胞需要在體外制備,這也讓該療法面臨成本高昂、難以規(guī)模化生產(chǎn)等困難,定價百萬是一個基礎(chǔ)門檻。
另一方面,CAR-T療法已經(jīng)連續(xù)四年沖擊國家醫(yī)保談判,但是與“國談”中“五十萬不談,三十萬不進”的隱形門檻相距甚遠,無果。
年治療費用動輒百萬,與國外已逐漸成熟的商保按療效付費、分段付費的邏輯,似乎也難以遷至國家醫(yī)保“保基本”的付費場景中。
如今,國產(chǎn)CAR-T療法,需要換個活法!出路在哪兒?適應(yīng)中國市場的多層次創(chuàng)新支付“門路”何在?
業(yè)界需要在“支持創(chuàng)新”和“保障制度的公平性”之間,為CAR-T此類“天價藥”找到醫(yī)保支付的突破口,就需要找到多層次創(chuàng)新支付的解決方案。這種反差,在2025年醫(yī)保“丙類”目錄發(fā)布的前夜顯得猶為具有深入討論的必要。
01、13款CAR-T,定價囧境
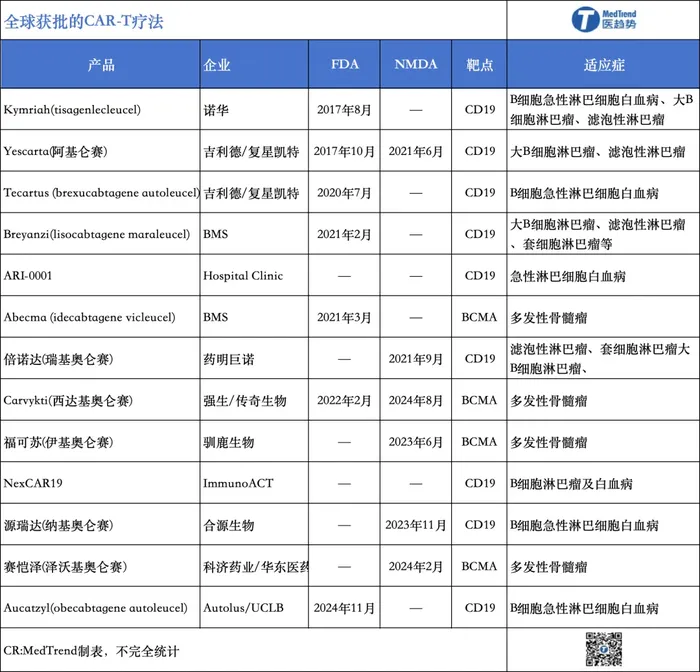
全球首款CAR-T療法是諾華Kymriah,于2017年8月獲批,隨后10月,吉利德Yescarta(阿基侖賽)上市,二者開啟了CAR-T療法商業(yè)化元年。
目前來看,全球已經(jīng)獲批的13款CAR-T療法。
從2024年最新數(shù)據(jù)來看,諾華Kymriah,吉利德Yescarta二者命運已截然不同。Kymriah銷售額跌至4.43億美元,黯然掉出領(lǐng)軍隊伍,退居第四。主要還是由于競爭對手的增多,Kymriah的市場份額也不斷被擠壓,導(dǎo)致下滑。
吉利德Yescarta在大B細胞淋巴瘤、濾泡性淋巴瘤領(lǐng)域的優(yōu)勢,開辟了第二增長曲線。2024年,Yescarta全球收入突破15億美元,連續(xù)8年蟬聯(lián)CAR-T“銷冠”。
2024年,強生/傳奇的Carvykti(西達基奧侖賽)潛能爆發(fā),在全球吸金近10億美元,躍居第二。BMS的Breyanzi也憑借多年穩(wěn)扎穩(wěn)打收獲7億美元,躋身第三。
中國市場,目前主要有6款CAR-T產(chǎn)品上市,有三款是CD19 CAR-T,另外三款是靶向BCMA。
復(fù)星凱特旗下阿基侖賽注射液是是國內(nèi)首個獲得上市批準的CAR-T細胞治療,上市于2021年6月,最初被批準用于治療既往接受二線或以上系統(tǒng)性治療后復(fù)發(fā)或難治性大B細胞淋巴瘤(r/r LBCL)成人患者,目前官方定價120萬元。
藥明巨諾旗下瑞基奧侖賽注射液是國內(nèi)第二款獲批上市的CAR-T療法,也是目前國內(nèi)唯一獲得三項適應(yīng)癥的批準的國產(chǎn)企業(yè),定價目前達到129萬元。
馴鹿生物的CAR-T于2023年6月獲批上市,是國內(nèi)首款獲得上市批準的BCMA CAR-T,定價116.6萬元。
其余還有合源生物的納基奧侖賽注射液是NMPA批準的第三款CD19 CAR-T細胞治療,也是國內(nèi)首個獲批治療B細胞急性淋巴細胞白血病的CAR-T,定價最低99.9萬元。科濟生物澤沃基奧侖賽注射液于2024年3月獲批,定價115萬元等。
02、國產(chǎn)CAR-T“難題”
國產(chǎn)CAR-T中,傳奇生物CAR-T產(chǎn)品Carvykti(西達基奧侖賽)最早于2022年在美國上市,一經(jīng)上市就在海外市場大獲成功。
2024年,其產(chǎn)品全球大賣9.63億美元,同比增長92.7%,距離10億美元的“重磅炸彈”標準,僅有一步之遙。
然而這款在美國定價46.5萬美元(約合人民幣330萬元)的抗癌藥,在中國市場卻“遇冷”。
2024年8月27日 ,傳奇生物西達基奧侖賽注射液(商品名:卡衛(wèi)荻?)正式獲得NMPA批準上市,成為國內(nèi)第6款上市的CAR-T細胞療法。
此次傳奇生物取消了中國的銷售和市場團隊,距離其西達基奧侖賽注射液上市不到1年時間!
有市場人士表示,在整體盈利目標下,傳奇生物更有可能選擇將有限資源投入回報更確定的海外市場。而CAR-T療法的商業(yè)表現(xiàn)一直低于預(yù)期的國內(nèi)市場,暫時還不是傳奇生物的重心所在。
此前,藥明巨諾發(fā)布2024年財報,全年營收1.58億元,同比下滑9%,虧損額為5.9億元。目前,藥明巨諾賬上現(xiàn)金只有7.57億元,按照這個虧損力度,撐不過兩年。
雖然目前藥明巨諾CAR-T已被列入超過80個商業(yè)保險產(chǎn)品,及102個地方政府的補充醫(yī)療保險計劃,但是2021年至2023年,藥明巨諾CAR-T瑞基奧侖賽輸注人數(shù)僅為30、141、168人,對應(yīng)業(yè)務(wù)收入分別為3079.7萬、1.46億、1.74億元。
2024年,藥明巨諾選擇將銷售費用提高24%,但收效甚微!
藥明巨諾的掙扎也揭示了一個殘酷現(xiàn)實,在現(xiàn)有支付體系下,CAR-T療法根本無法跑通國內(nèi)商業(yè)化閉環(huán)。
復(fù)星凱特在CAR-T的商業(yè)化困境與藥明巨諾存在相似性,盡管通過納入超過110款惠民保和80余項商業(yè)保險(如滬惠保最高賠付50萬元),患者自付比例仍超過50%,但保險覆蓋區(qū)域有限。
科濟藥業(yè)同樣暴露了CAR-T商業(yè)化面臨的共性困境。
其首款CAR-T產(chǎn)品賽愷澤(澤沃基奧侖賽注射液)定價115萬元/針,雖通過納入20余省市惠民保及商業(yè)保險(如滬惠保)覆蓋部分費用,但患者自付比例仍超50%。
盡管2024年銷售額達3943萬元,但公司凈虧損擴大至7.98億元,顯示高價未能轉(zhuǎn)化為盈利,支付難題成為核心障礙。
不同于傳奇生物直接短暫放棄國內(nèi)市場,為了破局,復(fù)星醫(yī)藥、科濟藥業(yè)選擇不同的策略。
復(fù)星醫(yī)藥推出“按療效支付”計劃(未達完全緩解最高返還60萬元),2024年已有近200名患者入組,CR率達58%,增強患者信心。科濟藥業(yè)聯(lián)合華東醫(yī)藥推動賽愷澤?通過“丙類目錄”提升商保覆蓋,并探索“按療效付費”模式(如未達完全緩解可部分退款),但政策落地仍需時間。
03、可能的解法
CAR-T療法一直以來以“天價藥”的身份出現(xiàn)在大眾視野中,
具體來看,Yescarta、Kymriah等產(chǎn)品國外的定價普遍在35萬美元和50萬美元之間,國內(nèi)復(fù)星凱特和藥明巨諾的定價分別為120萬元和129萬元,相對較便宜的納基奧侖賽注射液,售價仍高達99.9萬元。
高昂的價格與醫(yī)保“保基本”的定位天然沖突,過去幾年,藥企也試圖通過商保、分期付款等方式破局,但依然難以打開局面。
從120萬/針,到99.9萬/針,CAR-T療法的支付難題正在探索解法。
不過從當下來看,對于海外市場而言,至少前人有諾華、強生趟出了一條可行之路。對于國內(nèi)市場而言,與強生這樣的MNC合作,傳奇生物的CAR-T出海,為商業(yè)化難題找到了一個解法。
2022年2月,傳奇生物的CAR-T療法進入美國市場。
在美國,因為商業(yè)保險的充分參與,擁有CAR-T的藥企對其商業(yè)化有底氣。目前西達基奧侖賽在美國的定價,已經(jīng)從最初的46.5萬美元漲至54.97萬美元,是目前全球最貴的CAR-T產(chǎn)品之一。
當然了不止是傳奇生物,目前科濟藥業(yè)依托中美雙基地布局,尋求海外市場(如美國IND獲批)分攤研發(fā)成本;而復(fù)星凱特依托全球供應(yīng)鏈(如病毒載體國產(chǎn)化、自動化生產(chǎn)),推動降本增效,同時探索海外市場(如東南亞)以分攤研發(fā)成本。
不過,這條路看似簡單,但對于國內(nèi)藥企來說,要求或許會更高。
出海就意味著意味著投入巨大資金、資源推動全球多中心臨床,以此說服FDA。當然如果臨床數(shù)據(jù)足夠優(yōu)異,也可以像傳奇生物一樣,與強生的合作,讓其在海外臨床、產(chǎn)業(yè)化、銷售等方面沒了后顧之憂。
在真正的變革到來之前,國產(chǎn)CAR-T療法必須要想辦法先活下去。


