文|氨基觀察
誰會成為Claudin18.2靶點的“第一”,從來沒有太大懸念。臨床進度遙遙領先的安斯泰來,已經把優勢成功保持到了最后。
11月17日,安斯泰來宣布Claudin18.2抗體IMAB362,聯合化療治療Claudin18.2陽性、HER2陰性的,復發性轉移性胃癌的三期臨床成功:
不僅達到無進展生存期主要終點,同時達到總生存期的次要終點。
創新藥研發向來追求FIC,但對于Claudin18.2靶點來說,拿下“第一”可能遠遠不夠。
安斯泰來的IMAB362分子并不完美,導致其目前僅對Claudin18.2高表達患者有效,留下了大片空白的同時,也給后來者留出超車的機會。

面對難得的機遇,國內企業沒有放過,紛紛涌入Claudin18.2這一大靶點,不僅單抗、雙抗、CAR-T、ADC等多個技術同臺競技,甚至多家藥企同時參與多個技術路線的角逐。
隨著IMAB362三期臨床的成功,徹底打消了Claudin18.2靶點能否成藥的疑慮。接下來,就看國內藥企如何施展手段,對守擂者發起進攻。
01 不完美的FIC
對于創新藥來說,最高殿堂是FIC,但FIC并不意味著性能“完美”,通常來說依然有極大的改進空間,由此有了Me better、BIC藥物誕生的基礎。
某種程度上來說,安斯泰來的IMAB362,也是一款不完美的FIC。作為首個靶向Claudin18.2的單抗,其殺傷腫瘤細胞的主要機制為:
通過抗體的Fab段與腫瘤細胞表面抗原決定簇特異性結合后,再通過抗體Fc段與有FcγR的殺傷細胞(主要是NK細胞)等效應細胞結合,觸發效應細胞的殺傷活性,直接殺傷靶細胞。
根據機制來看,一款出色的Claudin18.2單抗需要具備的,是高效的結合腫瘤細胞和招募效應細胞的能力。
而IMAB362的缺陷正在于,其分子的親合力較弱,導致戰斗力受限。根據2期臨床數據來看,其療效受到患者腫瘤細胞Claudin18.2表達比例的牽制。
針對Claudin 18.2表達比例≥70%的患者,IMAB362+EOX方案(表柔比星+奧沙利鉑+卡培他濱)效果極為顯著:
實驗組的中位無進展生存期為9個月,中位總生存期為16.5個月;
對照組的中位無進展生存期為5.7個月,中位總生存期為8.9個月。
但針對Claudin 18.2表達比例介于40%—69%的患者,實驗組效果并不明顯,具體結果為:
實驗組中位無進展生存期為4.3個月,中位總生存期8.3個月;
對照組中位無進展生存期4.1個月,中位總生存期7.4個月。
很顯然,這一結果會讓IMAB362的受眾群體受到限制。
根據ClinicalTrials.gov,IMAB362聯合CAPOX作為晚期或轉移性胃癌及胃食管連接部癌一線治療的三期臨床,針對的只有Claudin18.2高表達(≥ 75%)患者。
如今,IMAB362三期臨床成功,的確給這部分胃癌患者帶來了治療新選擇。但除此之外,還有更多中、低患者有待新療法的出現。
在所有實體瘤中,Claudin18.2高表達患者僅占33%—37%。而在患者群體規模最大的胃癌領域,高表達患者占比更是僅有20%左右。

IMAB362的局限性,導致其難以惠及更多患者群體,這是國內企業后來居上的機會。
02 嘗試追趕的國內藥企
在國內,IMAB362追趕者不在少數。
單抗領域,創勝集團的TST001就在緊緊追趕IMAB362。目前,TST001中美III期臨床試驗正處于計劃階段。
根據分子結構設計來看,TST001與IMAB362有顯著差異。
一方面,TST001擁有與IMAB362不同的結合表位,最終具有兩大潛在優勢:與腫瘤細胞更高的親和力,以及和NK細胞更好的結合效率。
另一方面,創勝集團降低了TST001的Fc區域的巖藻糖含量,進一步增強了其與NK細胞上Fc受體的結合能力。
兩大改進,讓TST001擁有了具備超越IMAB362的潛力。如下圖所示,根據創勝集團研究,TST001的ADCC活性優于IMAB362。
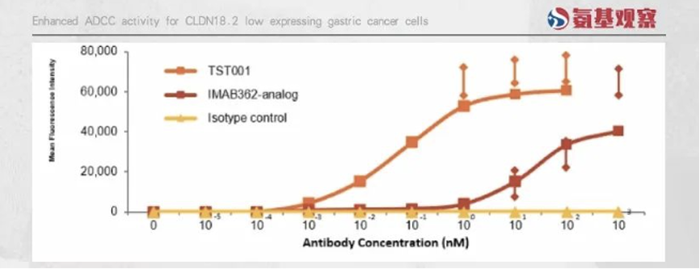
這一優勢讓TST001具備覆蓋Claudin18.2中表達患者的可能。根據今年9月創勝集團在ESMO公布的1期臨床數據,TST001針對中表達患者效果同樣突出。
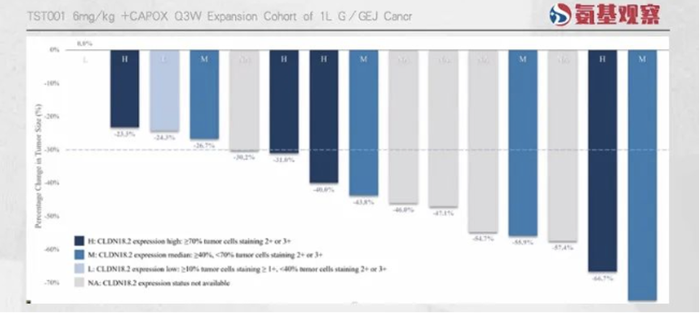
與此同時,創勝集團表示,未來還會在低表達患者中展開臨床研究。若TST001最終能夠覆蓋到中、低表達患者,無疑能夠超越IMAB362。
除創勝集團之外,包括奧賽康、天廣實、石藥集團、明濟生物、齊魯制藥等眾多國內藥企參與Claudin18.2單抗角逐戰。
這些選手的思路,大致一致,通過對Fc段改造等方式,增加對分子的親合力。
比如,奧賽康通過在分子設計和細胞株構件上采用去巖藻糖技術的方式,希望達到增強Claudin18.2單抗ASKB589的ADCC和CDC功能。目前,ASKB589正在開展I、II 期臨床試驗。
天廣實則是利用ADCC增強抗體平臺,對其Claudin18.2單抗MIL93的Fc段進行改造,使其與NK細胞上表達的FcγRIIIa具有更高的親和力的可能;
同時,公司使用噬菌體展示抗體篩選技術來提高MIL93與Claudin 18.2的親和力,最終希望帶來ADCC和CDC效應雙重增強的可能。
當然,大部分國內企業的Claudin18.2單抗臨床進展,都還處于早期階段。這些選手們的升級之路能否可行,有待后續數據的證明。
03 爭奪Claudin18.2至高點
在爭奪Claudin18.2至高點的征途中,入局的不僅有國產單抗,更有雙抗、ADC和CAR-T等眾多技術路線。
在Claudin18.2 ADC領域,國內企業則處于全球領先的身位。
如下圖所示,入局者包括信達生物、君實生物、康諾亞、德琪藥業等,其中榮昌生物、禮新醫藥產品都已進入臨床二期階段;而海外藥企的產品大都處于臨床一期階段。
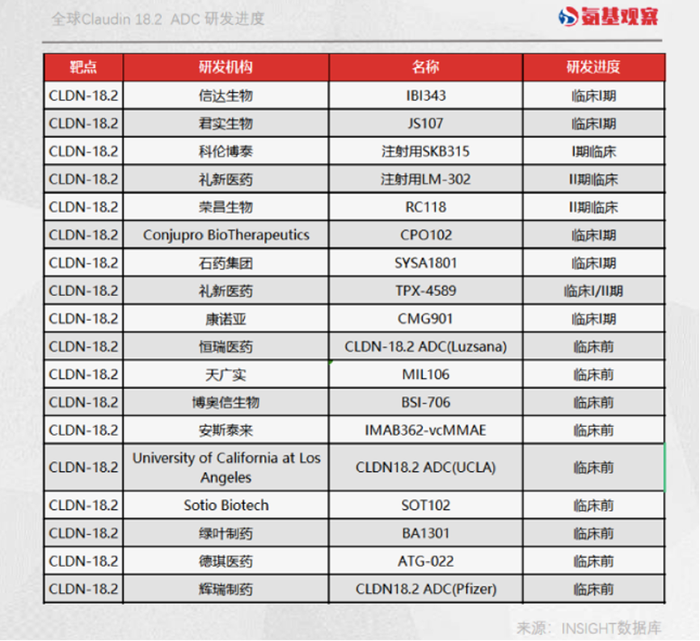
得益于全球領先的進度,國產Claudin18.2 ADC迎來出海潮:
先是今年5月份,禮新醫藥Claudin18.2 ADC成功授權給美國Turning Point,首付款+里程碑款總金額超10億美元。
緊接著,7月末科倫藥業和石藥集團的兩款Claudin 18.2 ADC,又相繼授權給大藥廠默沙東,及美國藥企Elevation Oncology。
ADC之外,靶向Claudin18.2的CAR-T研發領域,國內企業同樣占得先機。
目前,科濟藥業的CT-041針對晚期胃癌/食管胃結合部腺癌的研究,已經處于確證性Ⅱ期臨床實驗。
CT-041由經融合了人源化的抗CLDN18.2單鏈片段變體的CAR遺傳修飾的T細胞組成,因此具備有效靶向及消除在細胞表面表達CLDN18.2的腫瘤細胞的可能。
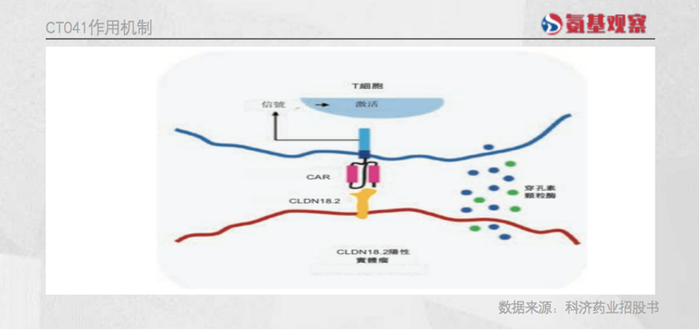
若后續臨床數據優異,CT-041也將成為潛力選手。
對于任何一個行業來說,“泡沫”本身并不可怕。凡事都有兩面性,資本在某個行業鼓吹“泡沫”的好處在于,能夠吸引大量資源投入,從而助推該行業快速發展。
某種程度上來說,國內創新藥行業正處于這一階段:雖然泡沫破滅,但仍在加速前進。國內藥企能夠在Claudin18.2靶點領域蓄勢待發,便是得益于此。
期待越來越多的國內藥企,在Claudin18.2靶點的爭奪戰中,帶來好消息。



