界面新聞記者 | 唐卓雅
界面新聞編輯 | 謝欣
7月4日,加科思發布公告稱,艾伯維基于資產組合與戰略決策原因,就雙方的許可及合作協議發出終止通知,該協議終止后,加科思將重新獲得之前授予艾伯維的SHP2抑制劑的全球權利。雙方將合作在180天內有序交接該協議項下的責任。在交接期間,艾伯維將繼續報銷預先批準的開發計劃下的所有費用。
也就是說,艾伯維選擇了“分手”,退回了加科思的SHP2抑制劑產品。
加科思表示,其仍在推進SHP2抑制劑的全球臨床開發計劃,包括KRAS G12C抑制劑等多種聯合療法和各種腫瘤驅動因子抑制劑的靶向療法。JAB-3312聯合Glecirasib(加科思KRAS G12C抑制劑)的臨床數據預計將于2023年下半年發布。
受此消息影響,7月5日加科思股價大跌。截至收盤,加科思報4.64元/股,股價跌24.52%。7月6日,加科思對界面新聞回應稱,重獲全球權益后,加科思將繼續推進SHP2全球臨床試驗,并將展開更靈活的聯合用藥。將重點布局SHP2與加科思自主研發的KRAS G12C抑制劑格來雷塞的聯合用藥試驗,日后也將推進SHP2與KRAS multi抑制劑(JAB-23400)的聯合用藥試驗。
而針對未來的現金儲備情況,加科思還表示,根據協議,雙方180天的交接期內,艾伯維將繼續報銷臨床試驗費用。在沒有新的資金進賬的情況下,加科思現金生命周期為2年。此外,加科思管線中有多個項目具有license out的潛力,也會根據市場情緒擇時融資。
雙方此次合作前后共三年。2020年6月,艾伯維與加科思簽訂一份總價值高達8.55億美元的license out(對外授權)協議,宣布達成全球戰略合作,共同開發和商業化SHP2抑制劑。
根據協議約定,艾伯維獲得SHP2產品組合的獨家許可權,加科思則繼續開展抑制SHP2活性的口服小分子藥物JAB-3068和JAB-3312的早期全球臨床研究,相關研發費用由艾伯維承擔。SHP2在中國以外的銷售額約80%歸屬艾伯維所有。
靠這項合作,加科思在2020年產生4.86億元的收入,2021年和2022年的營收也分別在9574.6萬元、1.53億元。
加科思在招股書也提到,該合作有助于化解候選藥物的風險,確保在全球范圍內最大程度實現其臨床和商業價值。
至今,艾伯維累計支付加科思的首付款8.55億美元,及2021支付給加科思的2000萬美元的首筆里程碑付款,加科思已從這項合作獲益8.75億美元,合計人民幣約63.29億元。
雖然從財務上看,加科思也賺了不少,但其SHP2產品組合的海外市場前景顯然要暗淡了很多。
加科思是一家臨床階段制藥公司,專注于全球首創新型腫瘤療法的自主發現和開發,其創始人王印祥博士曾是貝達藥業共同創始人之一,目前加科思有5款管線(KRAS G12C、SHP2、BET、Aurora A、CD73)處于臨床階段。
SHP2抑制劑屬于加科思目前的核心產品。作為RAS信號通路中的關鍵信號轉導節點,SHP2可以促進癌細胞增殖,并在對靶向療法產生耐藥性中發揮重要作用。SHP2抑制作為單藥療法可能對具有特定改變的癌癥有效,與各種致癌驅動因子的抑制劑聯合使用時,可以在規避耐藥性方面發揮重要作用。
迄今為止,全球尚無獲批準或上市的SHP2抑制劑。據藥渡數據,全球在研SHP2抑制劑在研數量超30個,大多處于臨床前階段,最快處于2期臨床。目前已有15款SHP2抑制劑進入臨床試驗階段,其中BBP-398、TNO-155等6款已進入2期臨床。
中郵證券在2022年年底發布的一份研報稱,SHP2抑制劑聯用潛力備受關注,海外主要在研SHP2抑制劑均完成對MNC授權。
在先導化合物SHP-009和變構口袋(tunnel口袋)的基礎上,諾華和其他4家藥企(加科思、Relay、Revolution、BridgeBio)分別開發出自有的SHP2抑制劑候選藥物。上述4家藥企的SHP2抑制劑均已授權給MNC,首付款在4500萬-9000萬美元之間。
不過,與艾伯維同加科思“分手”一樣,去年12月,賽諾菲也已與Revolution終止合作。

國內也已有多家藥企布局SHP靶點,如諾誠健華、圣和藥業、貝達藥業、凌濟生物、奕拓醫藥等。國內10款SHP2抑制劑處于臨床階段,加科思的JAB-3312和JAB-3068進度最快。
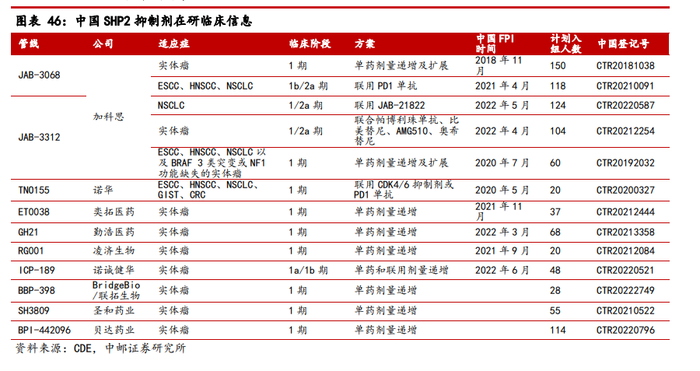 此外,中郵證券發布的研報還提及,SHP2抑制劑主要適應癥的中國潛在市場為54億元。未來,重獲SHP2全球權利的加科思的商業潛力或許將大大增強。
此外,中郵證券發布的研報還提及,SHP2抑制劑主要適應癥的中國潛在市場為54億元。未來,重獲SHP2全球權利的加科思的商業潛力或許將大大增強。
除了SHP2之外,加科思目前其他的產品研發進展順利。在中國,攜帶KRAS G12C突變的NSCLC患者的關鍵試驗已于2022年9月獲藥品審評中心(CDE)批準。2022年12月,Glecirasib已獲CDE授予用于治療KRAS G12C突變的晚期或轉移的NSCLC患者的二線及以上治療的突破性治療藥物認定。
值得一提的是,加科思在研發上投入重金,研發成本逐年增加。2018年至2022年,加科思的研發投入分別為8488.7萬元、1.39億元、1.86億元、2.81億元、4.46億元。但巨大的研發投入也使得加科思連年虧損。2018年至2022年,加科思凈虧損分別為1.56億元、4.26億元、15.14億元、3.01億元、3.71億元。此外,加科思在年報中提及,虧損原因還包括行政開支及具優先權的金融工具的公允價值虧損。
而加科思近三年的收入來源較為單一,加科思在年報中提到,公司營收主要來自于與艾伯維的SHP2抑制劑合作協議所產生的研發成本報銷,一旦合作終止,加科思龐大的研發成本是否會影響公司的可持續發展。