文|化妝品觀察
2023年行將結束,行業基本大法《化妝品監督管理條例》施行至今也已三年,這期間,化妝品法規監管體系的“四梁八柱”基本搭建完成,“合規”兩個字也被擺上了史無前例的重要位置。
而在即將到來的2024年,行業又將面臨一系列新的“考驗”,如,1月1日起新注冊備案產品需提交全部原料的安全信息資料,5月1日后需提交完整版安評報告。
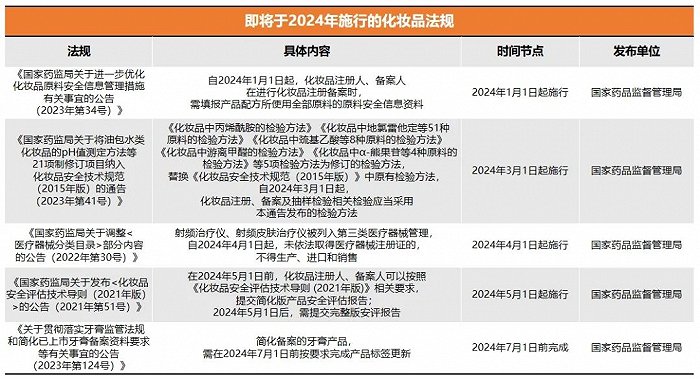
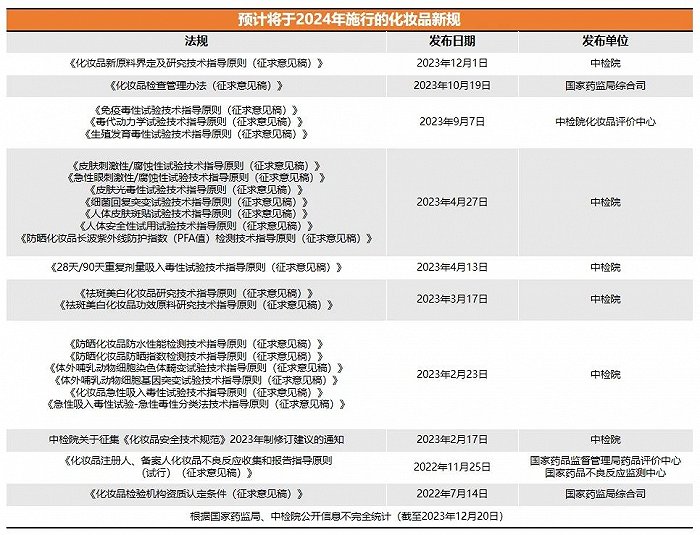
與此同時,《化妝品檢查管理辦法(征求意見稿)》等新規正在征求意見階段,大概率將在2024年落地施行,這意味著,化妝品行業合規發展正式進入“深水區”。
新規倒逼行業升級,新的一年,品牌、工廠乃至一直游離在化妝品法規之外的原料商,都將在“陣痛”中迎來巨變。
01、監管大網收緊,原料進入“身份證”時代
根據國家藥監局發布的《關于進一步優化化妝品原料安全信息管理措施有關事宜的公告(2023年第34號)》(下稱《公告》),自2024年1月1日起,化妝品注冊人、備案人進行注冊備案時,應當按照相關法規、技術規范,填報產品配方所使用全部原料的安全信息資料;2021年5月1日前注冊備案的化妝品中所含《化妝品安全技術規范》相關原料,以及2021年5月1日至2023年12月31日期間注冊備案的化妝品中具有防腐、防曬、著色、染發、祛斑美白功能的原料,需在2024年1月1日前補報相關原料的質量規格證明或者原料安全信息資料。

▲《關于進一步優化化妝品原料安全信息管理措施有關事宜的公告(2023年第34號)》
一直以來,填報原料安全信息壓得不少企業喘不過氣,原料商不配合、原料信息不一致、系統操作復雜等,是擺在不少企業面前的難題。
基于此,《公告》進一步延長過渡期,將新品需提供配方中全部原料安全相關信息的時間點,從“2023年1月1日起”延期至“2024年1月1日起”;由原來全部原料強制性提供附件14或報送碼,改為允許其他原料的原料安全信息資料由注冊人、備案人存檔備查。與此同時,注冊人、備案人可以選擇關聯原料商提供的報送碼,也可以選擇采取自行填報原料安全信息資料的方式進行報送。
“監管層考慮到企業困難已放松要求,若企業至今還未做好準備,就只能自我反思了。”某企業研發工程師建議,對于老品,要考慮補交的原料安全資料與注冊備案信息是否一致,實際生產配方和注冊備案信息是否一致等問題,若無法保證一致,應及時注銷,清庫存;對于新品,要對原料生產商提供的報送碼及相應的原料安全資料進行審核,確保信息一致性,且符合完整版安評報告的相關要求。
“對原料進行合規化監管是大勢所趨。”某資深法規人士分析,原料的安全是產品安全的前提,縱觀這一年我國多起化妝品公共衛生突發事件,如嬰兒毒面霜、汞中毒事件,都與化妝品原料密不可分。
他提醒,監管趨嚴,化妝品企業承擔著不良反應監測、飛檢抽檢風險,“不要想著作假,提供虛假資料蒙混過關,這都是給自己挖坑”。
02、完整版安評來襲,行業“洗牌”加劇
2021年4月國家藥監局發布的《化妝品安全評估技術導則(2021年版)》(簡稱《技術導則》)明確要求,自2022年1月1日起,化妝品注冊人、備案人在進行化妝品注冊或備案時,需按照《技術導則》的要求提交產品的安全評估資料。在2024年5月1日前,可提交簡化版的產品安全評估報告;在2024年5月1日后,需提交完整版的產品安全評估報告。
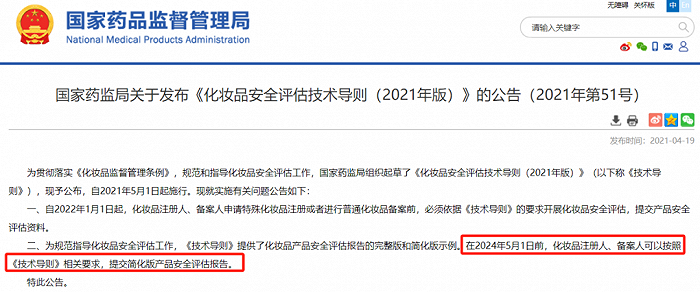
▲截自國家藥品監督管理局官網
相較于簡化版安評報告,完整版安評報告增加了防腐劑挑戰報告、產品的理化特性/穩定性檢測報告以及產品與包裝材料的相容性檢測報告,且不可再引用“已使用原料目錄中收錄的原料最高使用量”和“本企業的歷史使用濃度”作為評估的證據。
化妝品安全評估是一項涉及毒理學、化學、物理學、醫學等的綜合技術,而完整版安評報告所涉及的程序更復雜,專業性更高。據《化妝品觀察》了解,提交完整版安評報告對于不少企業而言是座難以跨越的“大山”,面臨原料毒理學數據缺乏、安全評估人才短缺、國內原料標準差異以及安全評估能力不足等難題。
最為關鍵的是,目前至少有60%的原料需要通過搜集毒理學終點或加測毒理學試驗來完成安全評估,尤其是植提、發酵以及生物合成的一些原料。原料有了毒理數據,方能支撐整個產品的安全評估。但毒理學實驗成本高、周期長,無論是原料商、檢測機構還是品牌方,都面臨著嚴峻的考驗。換言之,品牌方、工廠或受限于原料而無法開展完整版安評工作,進而導致開發新品受阻。
雖然在過去一年,中檢院相繼發布了公開征求《免疫毒性試驗技術指導原則(征求意見稿)》等技術指導原則意見的通知,進一步明確了毒理檢測方法,為企業提交完整版安評鋪路。但在行業人士看來,就算官方明確了毒理檢測方法,但高達百萬的檢測費用也會讓企業望而卻步。
“若如期施行,那些無法進行安全評估的原料就只能放棄了。”某研發工程師無奈表示,這將在行業掀起新一輪風暴。
不少業內人士呼吁,我國化妝品安評工作起步晚、基礎薄弱,希望再給予企業2~3年緩沖過渡期,最好由國家牽頭,原料商主導,工廠、品牌企業全力配合,共同來完成安全評估工作。
03、熊果苷等原料明確檢驗方法,美白劑清單呼之欲出
2023年8月28日,國家藥監局發布了《關于將油包水類化妝品的pH值測定方法等21項制修訂項目納入化妝品安全技術規范(2015年版)的通告》,其中《化妝品中丙烯酰胺的檢驗方法》《化妝品中地氯雷他定等51種原料的檢驗方法》《化妝品中巰基乙酸等8種原料的檢驗方法》《化妝品中游離甲醛的檢驗方法》《化妝品中α-熊果苷等4種原料的檢驗方法》等5項檢驗方法為修訂的檢驗方法,替換《化妝品安全技術規范(2015年版)》中原有檢驗方法,自2024年3月1日起,化妝品注冊、備案及抽樣檢驗相關檢驗應當采用本通告發布的檢驗方法。
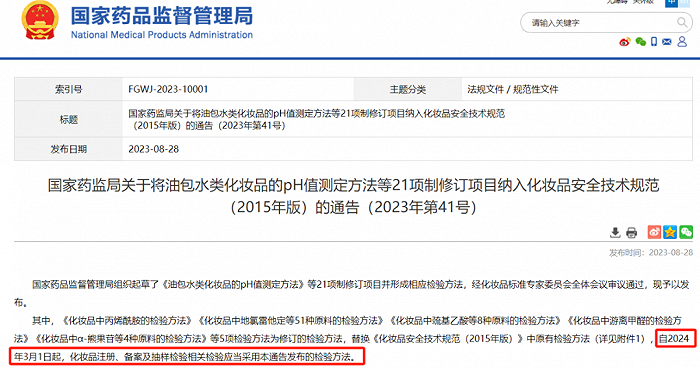
▲截自國家藥品監督管理局官網
一直以來,因具備美白功效,熊果苷風靡美妝市場,近年來熱度不斷攀升。不過,此前的《化妝品安全技術規范(2015年版)》,并未收錄α-熊果苷和熊果苷的測定方法,僅收錄了禁用成分氫醌和苯酚的測定方法,且該方法檢出濃度不能滿足監管需求。這無疑給熊果苷的運用留下了隱患。
如今,《化妝品中α-熊果苷等4種原料的檢驗方法》規定了測定化妝品中α-熊果苷、熊果苷、氫醌和苯酚含量的檢驗方法,以及熊果苷常見雜質的檢測方法,無疑堵住了這一“漏洞”。
“熊果苷的添加亂象要結束了。”恩特科技負責人表示,雖然祛斑美白劑清單尚未公布,但檢測方法先行出臺,意味著企業進行相關檢測有了官方指導方法,也意味著監管層未來會對這類美白原料的添加量加強監管。
“老產品要自查自糾,新產品要采用新檢驗方法,含有相關原料的產品,不管是功效或關鍵原料的實際濃度含量還是風險物質的殘留量,盡量在采購原料前要求原料商提供檢測報告,或者內部送檢加測,避免違規添加而踩坑。”綠翊(廣州)技術服務有限公司總經理鐘柱宏提醒,隨著禁用原料和限用、準用原料的檢測方法不斷完善,后期監管層對相應項目市場抽檢的概率也會增加,建議企業重視原料安全,提前規避風險。
值得一提的是,早在2023年2月17日,中檢院便下發了關于征集《化妝品安全技術規范》2023年制修訂建議的通知,征集截止時間為2023年3月17日。多位業內人士指出,《化妝品安全技術規范(2015年版)》自實施以來,已經過多次修訂,相信更完善、更科學的新版《化妝品安全技術規范》將在2024年與大家見面。
04、納入“械字號”陣營,美容儀結束“野蠻生長”
2022年3月國家藥監局發布《關于調整〈醫療器械分類目錄〉部分內容的公告(2022年第30號)》(簡稱《公告》),明確指出,射頻治療儀、射頻皮膚治療儀類產品按照第三類醫療器械管理,自2024年4月1日起,未依法取得醫療器械注冊證不得生產、進口和銷售;未取得醫療器械生產、經營許可(備案)的企業,不得從事相關產品的生產和銷售。
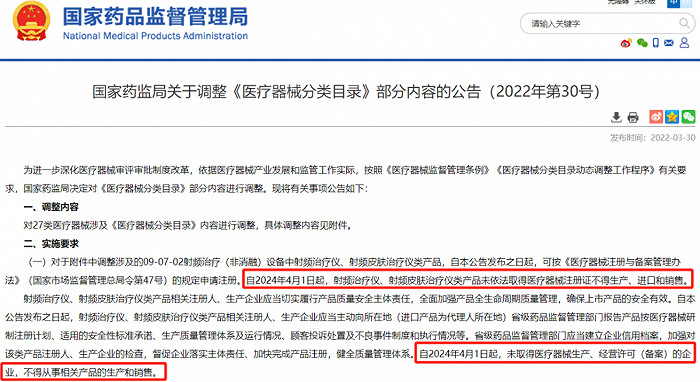
▲截自國家藥品監督管理局官網
值得關注的是,2023年4月10日國家藥監局器審中心發布《射頻美容設備注冊審查指導原則》,進一步指出,射頻美容設備包括手持式(小型)設備,即家用美容儀。
這意味著,原本參照家電行業管理的家用美容儀,自2024年4月1日起,須取得第三類醫療器械注冊證方能上市銷售。簡言之,美容儀正式被納入“械字號”陣營。
據悉,正常三類醫療器械注冊,從臨床備案、試驗完成、注冊提交及至受理下證,整個審批周期接近2年。早在《公告》頒布之時,某業內人士便直言,光是開展人體臨床試驗這項要求,便將不少品牌拒之門外,“家用射頻美容儀市場將告別野蠻生長,迎來新一輪‘大洗牌’”。
此言非虛,嗅覺敏銳的企業已紛紛采取行動。一邊是積極“持證”上崗,如中國美容儀品牌OGP、AMIRO覓光相繼申報了臨床試驗項目;另一邊則是洗手收攤,上演最后的狂歡,如寶潔關閉旗下美容儀品牌OPTE,包括知名美容儀品牌Refa在內的品牌,則價格腰斬進行清倉大甩賣。
只有退潮后,才能真正看清誰在裸泳。留給企業的時間不多了,上述業內人士表示,“三個月后,市場上魚龍混雜的美容儀產品將面臨下架,美容儀市場正式迎來新的局面”。
05、牙膏標簽過渡期結束,消耗庫存包材迫在眉睫
根據國家藥監局發布的《關于貫徹落實牙膏監管法規和簡化已上市牙膏備案資料要求等有關事宜的公告(2023年第124號)》,簡化備案的牙膏產品,標簽標注的內容符合《化妝品監督管理條例》《牙膏監督管理辦法》(下稱《辦法》)和《化妝品標簽管理辦法》等規定要求,僅標簽標注的格式等需要進行規范調整的,可以在簡化備案時使用已上市的銷售包裝標簽,并在2024年7月1日前按要求完成產品標簽更新。

▲截自《關于貫徹落實牙膏監管法規和簡化已上市牙膏備案資料要求等有關事宜的公告(2023年第124號)》
《辦法》已對牙膏產品標簽應當標注的內容、禁止標注的內容做了明確的規定。與此同時,兒童牙膏(適用年齡為12歲及以下)還應在銷售包裝展示面標注兒童標志“小金盾”,把標志文字“兒童化妝品”改為“兒童牙膏”,并標注“不能食用”“謹防吞咽”等警示用語。
《辦法》已于2023年12月1日起施行,但符合要求的簡化備案牙膏產品,可以繼續使用已上市的銷售包裝標簽直至2024年7月1日。
公開資料顯示,截至2022年底,全國取得生產許可證的牙膏企業共218家,牙膏年產量達60余萬噸,其中本土企業占比為52%。而在2023年12月1日前,我國97%的牙膏產品已完成簡化備案。
“避免了‘一刀切’,對于已上市老產品的包裝標簽給予了合理的過渡期,利好企業。”某牙膏品牌負責人透露,這意味著企業可以在過渡期內繼續消耗庫存的老包材,減少了損失。
某資深法規人士則提醒道,牙膏企業的舊包材必須在2024年7月1日前消耗完,并著手進行標簽更新,“明年7月1日后,舊包裝就不合規,只能報廢了”。


